پی اچ چیست؟ – نحوه محاسبه پی اچ

در این مقاله قصد داریم شما را با موضوعاتی مثل پی اچ چیست؟، چه کاربردهایی دارد، بیان تاریخچه آن، بازه اندازهگیری پی اچ، تاثیر دما روی پی اچ، چگونگی محاسبه ph، انواع مواد و پارامترهایی که نیاز به اندازهگیری پی اچ دارند و تاثیرات عوامل محیطی بر روی میزان pH و … آشنا نماییم. در ادامه همراه هانا ایران باشید تا هر آنچه لازم است در این حوزه بدانید را به شما آموزش دهیم.
فهرست مطالب موجود در مقاله:
- پی اچ چیست؟
- بازه اندازهگیری پی اچ
- تاثیر دما روی پی اچ
- چگونگی محاسبه ph
- انواع موادی که نیاز به اندازهگیری پی اچ دارند
- تاثیر عوامل محیطی بر روی پی اچ
در نوشتهها و خیلی از مطالعههای شیمی، برای گفتن خاصیت بازی یا اسیدی بودن یک محلول آبی یا بقیهی محلولهای مایع این کلمه ( PH ) را به کار میبرند. این کلمه نیز به صورت عظیم در کشاورزی و بیولوژی مورد استفاده قرار میگیرد. و به بیان دیگر، PH یک محلول، مقدار غلظت یون هیدروژن محلول در آن میباشد که توسط یک مقیاس با این عنوان تعریف میشود.
این واژه در حقیقت اصطلاحی بوده که منظور آن اسید و باز هستند. مادهای که پس از حل شدن در آب باعث رها سازی یون هیدروژن ( H+ ) میشود اسید نام دارد. طعم اسیدها اغلب ترش است و بیشترمواد مغذی شامل PH اسیدی میباشند.
به مادهای که پس از حل شدن در آب باعث رها سازی یون هیدروکسید ( OH– ) میشود باز میگویند. طعم این مواد اغلب تلخ و گس هستند.
با توجه به مقایسه انجام شده پی اچ، آن دسته از موادی که دارای PH پایین تر از 7 هستند اسیدی و آن دسته که بیشتر از 7 باشند قلیایی هستند.
اسیدهای خوراکی
اگر بخواهیم چند اسید خوراکی را اسم ببریم میتوانیم به آبلیمو، سرکه، آب پرتقال یا افشره، نوشابههای گازدار و گوجه فرنگی اشاره کنیم.
مواد بازی
چند نمونه از مواد باز آشنا آب دریا، صابون و مایع سفید کننده میباشند.
بر اساس طبیعت لگاریتمی پی اچ، حتی تغییرات کوچک در آن شایان توجه میباشند. در حقیقت فرق میان PH 6 و PH5 میزان غلظت اسید را ده برابر بالا نمایش میدهد. توجه کنید که تنها 0.3 تغییر باعث دو برابر شدن میزان غلظت اسید میشود. مزه، فاسد نشدن و قوام مواد مغذی میتوانند با توجه به تغییرات PH تاثیراتی را از این تغییر دریافت کنند.
کاغذ پی اچ چیست؟
این کاغذ نوعی معرف میباشد که از طریق تغییر رنگ، مقدار بازی، اسیدی و یا حنثی بودن یک فضا و ماده را عموما در رنگهای نارنجی و قرمز نمایش میدهد که اکثر آزمایشگاهها آن را به کار میگیرند، این کاعذ اسمهای زیادی همچون کاغذ پ هاش، کاغذ پی اچ یا کاعذ PH دارد.
پی اچ مادهای است که در مقیاسی بین اعداد صفر تا 14 قرار دارد که عدد 7 خنثی بودن آن را نشان میدهد.
در صورتی که عددی پایین تر از 7 باشد فضای اسیدی را نشان میدهد و اگر این عدد بیشتر از 7 باشد فضا یا محیط بازی را نشان میدهد.
کاغذهای پی اچ و چگونگی استفاده آنها
این کاغذها که برای مشخص کردن پی اچ محلولها به کار گرفته میشوند در نمونههای کاغذ پی اچ، کاغد تورنسل و یا لیتموس وجود دارند که فروش آنها در بازار تکی و یا به شکل رولی میباشد. البته دقت کنید که بعضی از انواع این کاغذها تنها نشان دهنده فضاهای اسیدی هستند و بعضی تنها نشان دهنده فضاهای بازی میباشند.
نوع تاثیر این سه نمونه کاغذ هم تا حدودی با یکدیگر فرق میکند. به این صورت که نوع لیتموس و تورنسل تنها بازی یا اسدی بودن محلول را نشان میدهند ولی نوع پی اچ کمی متفاوت است و در کنار نمایش اسیدی یا بازی بودن محلول، اندازه و مقدار بازی یا اسیدی بودن فضا را هم با استفاده از جدول راهنمایی که با خود دارد و درجه بندی شده است نشان میدهد.
برترین و با کیفیت ترین نوع این کاغذها محصولات آلمانی هستند که میتوانید در بازار آنها را در بستههای 100 عددی استریپ پیدا کنید.
دقت کنید که در بازار کاغذ پی اچ با عنوانهای دیگری هم مثل پی اچ سنج و….. به فروش میرسد که لازم است آن را وارد محلول کنید و رنگ آن پس از کمی انتظار عوض میشود.
تاریخچه پی اچ
پس از توضیح پی اچ چیست و کاغذ پی اچ چیست حال به تاریخچه آن میپردازیم.
در سال 1909 میلادی برای اولین بار یک دانشمند دانمارکی به اسم “اس پی ال سورانسن” یک مقیاس با عنوان PH ایجاد کرد. و با توجه به تفاسیر و اندازهگیریهایی که در سلولهای الکتروشیمیایی وجود دارد در سال 1924 برای مطابقت با آن تفاسیر و اندازهگیریها دوباره برای تعریف آن تجدید نظر کردند. در واژه PH حرف P دقیقا معلوم نیست چه مقصودی دارد و درباره آن بحث وجود دارد، به دلیل اینکه سورانسن به شکل شفاف تعیین نکرده که دلیل استفاده اش از این حرف چه بوده است. او شیوهای را برای اندازهگیری اختلاف پتانسیل (Potential) توضیح داده که اشاره میکند غلظت یونهای هیدروژن با توان (Power) 10میباشد. از این رو حرف P ، هم ممکن است به منظور واژه Power باشد و هم ممکن است به عنوان واژه Potential شناخته شود. حتی امکان دارد سورانسن به شکل فرضی نام محلول آزمایشی را P و نام محلول مرجع را q گذاشته باشد.
ابزارهای اندازه گیری پی اچ
برای اندازه گیری میزان عملکرد هیدروژن– یونی در محلولهای گوناگون از یک وسیله علمی که یکی از ابزارهای لازم آزمایشگاهی در آزمایشگاههای گوناگون میباشد به نام پی اچ متر استفاده میکنند. این ابزار آزمایشگاهی که یک وسیله الکتریکی و یکی از اصلی ترین ابزارآلات آزمایشگاهی میباشد همواره جهت اندازه گیری و حساب کردن PH نمونهها با هدف کشف بازی یا اسیدی بودن مواد استفاده میشود.
پی اچ متر نشان دهنده یک کمیت لگاریتمی به کاربر میباشد. این ابزار همچنین به اندازه گیری تفاوت در پتانسیل الکتریکی بین یک PH الکتریکی و الکترود مرجع میپردازد. به این خاطر است که بعضی اوقات این ابزار را پتانسیومتریک هم نام میبرند. تفاوت الکتریکی بودن هم به قلیایی یا اسیدی بودن مایعات ربط دارد. ابزار آزمایشگاهی پی اچ متر را به طور معمول در آزمایشهای آزمایشگاههای گوناگون و کنترل کیفی به کار میبرند.
موارد کاربرد پی اچ متر
یکی از اساسی ترین کاربردهای این ابزار آزمایشگاهی، استفاده آن جهت حساب کردن و اندازه گیری مقدار قلیایی و اسیدی بودن مواد (میزان یون هیدروژن) در کسب و کارهایی مانند داروسازی، دامپروری، کشاورزی، مراکز پزشکی، صنایع غذایی، مراکز آزمایشگاهی و تصفیه خانهها میباشد.
نحوه عملکرد پی اچ متر
نحوه عملکرد این ابزار به طوری میباشد که با اندازه گیری پتانسیل الکتریکی (بین دو الکترود از نمونه) میتواند یون H (هیدروژن) را اندازه گیری کند و سرانجام قلیایی یا اسیدی بودن محلول را تعیین کند. البته دقت کنید که هماکنون نمونههای پیشرفته تری از این ابزار مانند پی اچ متر دیچیتالی ساخته شده است که جهت اندازه گیری مقدار PH که در مواد وجود دارد، این دستگاه به همراه مدار الکترونیکی (از یک الکترود شیشهای و خارجی یا الکترود ترکیبی و ولتمتر تشکیل شده است) مورد استفاده قرار میگیرد.
انواع پی اچ متر یا اسید سنج
- پی اچ متر قلمی
- پی اچ متر پرتابل
- پی اچ سنج رومیزی
برای مشاهده انواع پی اچ متر کلیک کنید.
پی اچ آب
دامنهی پی اچ در آب دریا عددی میان 7.5 تا 8.4 میباشد. از طریق این مقیاس، تاثیر ویژهای در چرخه کربن ایجاد میشود. با توجه به خاصیتهای شیمیایی که آب دریا دارد تعیین پی اچ آب اندکی سخت و باعث شده تا برای آن مقادیر گوناگونی را در نظر داشته باشند.
پی اچ خاک
امکان دستیابی به عناصر غذایی در خاک توسط پی اچ خاک مشخص میشود. برای بیشتر گیاهان زراعی، پی اچ مرغوب عددی بین 6 الی 7 میباشد. عواملی مانند فضا و وضعیت آب و هوایی، کیفیت خاک و ترکیبات آن، کیفیت آب و کودهای شیمیایی همگی در پی اچ خاک نقش دارند و میتوانند در میزان موفقیت یا موفق نشدن یک گیاه در آن ناحیه تاثیرگذار باشند. بارش باران و تجزیه مواد آلی باعث تنزل پی اچ خاک میشوند. برای مثال در نواحی بسیار مرطوب و دارای بارندگی به خاطر شسته شدن کاتیونهای بازی، خاک شکل اسیدی میگیرد و در مقابل خاکها در نقاط گرم و خشک غالبا قلیایی میباشند. ریشه در خاکهای اسیدی به طور طبیعی به میزان پایین تری رشد و پیشرفت دارد. باکتریها در خاک قلیایی و قارچها در خاک اسیدی رشد بهتری دارند.
وزارتخانه کشاورزی سرویسهای مراقبت از منابع طبیعی ایالات متحده آمریکا (United States Department of Agriculture NRCS) مقدار PH در خاک را به شکل زیر ترتیب بندی کرده است. در پایین نیز چگونگی تغییر عناصر غذایی خاک را با توجه به نوع تغییرات PH خواهید دید.
- اسم: دامنه تغییرات PH
- فرا اسیدی: 3.5>
- اسیدی شدید: 4.4- 3.5
- اسیدی خیلی قدرتمند: 5.0- 4.5
- اسیدی قدرتمند: 5.5- 5.1
- اسیدی ضعیف: 6.0- 5.6
- کمی اسیدی: 6.5- 6.1
- خنثی: 7.3- 6.6
- کمی بازی: 7.8- 7.4
- بازی ضعیف: 8.4- 7.9
- بازی قدرتمند: 9.0- 8.5
- بازی خیلی قدرتمند: 9.0<
برای مشاهده ph سنج خاک کلیک کنید.
تغییر پی اچ خاک
در ادامه مقاله پی اچ چیست میخواهیم بپردازیم به چگونگی تغییر پی اچ خاک. اگر بخواهیم خاک را اسیدی کنیم باید به آن گوگرد بیفزاییم. مواردی مانند نیترات آمونیوم، سولفات آلومینیوم، سولفات آهن و سولفات آمونیوم نیز در تنزل پی اچ تاثیرگذار هستند.
برای قلیایی کردن خاک، باید کربنات کلسیم یا آهک به آن بیفزاییم. محصول هوکر میتواند نقش بافر را بازی کند به معنای تبدیل خاکهای قلیایی به اسیدی و خاکهای اسیدی به قلیایی.
شناساگرها
برای مشخص کردن PH محلولها، شناساگرها به کار گرفته میشوند. در فضاهای بازی یا اسیدی، شناساگرها رنگهای گوناگونی به خود میگیرند. شناساگرها انواع مختلفی دارند که به چند شناساگر شناخته شده در ادامه میپردازیم.
- کاغذ تورنسل (لیتموس)
- محلول متیل اورانژ
- محلول متیلن بلو
- محلول فنول فتالئین: در صورتی که فنول فتالئین را در یک محلول بازی بریزید، محلول را به رنگ ارغوانی در میآورد.
- گلبرگ گل سرخ
دقت کنید که اگر از شناساگرهای شیمیایی استفاده کنید زمان بر بوده و برای مشخص کردن دقیق PH غلطهایی به وجود میآید. به همین خاطر است که برای مشخص کردن PH به سراغ PH سنج دیجیتالی میروند.
الکترودهای pH

الکترود های pH با تکنولوژی روز دنیا (تولید و طراحی هانا)
هانا بزرگترین تولید کننده تجهیزات آزمایشگاهی، و بزرگترین تولید کننده الکترود در اروپاست. کمپانی هانا با توجه به ابداعات خود تا کنون به پیشرفت این صنعت کمک شایانی نموده است.
در سال ۱۹۸۱، هانا فرمولاسیون خودش را برای ساخت شیشه استفاده شده در تولید الکترود با کمک موسسه آزمایشگاهی شیشه در مورانو ایتالیا ابداع نمود. از این لحظه به بعد، شرکت به ساخت این الکترودهای شیشهای برای سنجش pH مشغول است.
در حالی که سایر شرکتها میزان تولید خود در این زمینه را کاهش دادند، هانا پیوسته خط تولید الکترود خود را توسعه داده است تا بتوانند پاسخگوی نیاز رو به گسترش بازار به محصولات و الکترود های منحصر به فرد خود باشد.
این شرکت جهت افزایش کارکرد و زمان نگهداری الکترود های خود رنج وسیعی از محلولهای تمیز کننده و نگهداری را نیز عرضه نموده است تا الکترودها را پیوسته در بهترین شرایط عملکردشان قرار دهد.
تولید الکترودهای pH
دیگر تولید کنندگان الکترود پیوسته از تکنیکهای همجوشی در کورههای القائی استفاده میکنند در این عمل، شیشه ساعتها در معرض دمای همجوشی قرار دارد، و به سختی میتوان کیفیت محصول را کنترل نمود زیرا بعضی از مواد موجود در شیشه در دمای بالای همجوشی تبخیر میشوند. هانا از تکنولوژی دمیدن در شیشه استفاده میکند که متخصصان مورانود در ایتالیا توصیه نموده اند.
میلههای شیشهای حساس بصورت کنترل شده ذوب میشوند. فقط در این روش است که شیشههای حساس فقط برای چند ثانیه در دمای بالای همجوشی قرار میگیرند و تنها در این روش است که میتوان کیفیت محصول نهایی را تضمین نمود.
تئوری و چگونگی سنجش pH
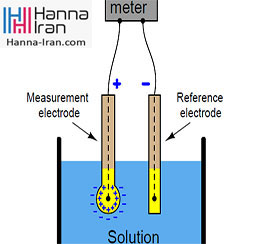
رایجترین شیوه سنجش pH استفاده از الکترودهای شیشهای است. این الکترودهای pH شامل یک سنسور pH (که ولتاژ آن متناسب با فعالیت یون هیدروژن موجود در محلول فرق میکند)و یک الکترود مرجع (که ولتاژ مرجع و ثابتی را بصورت پیوسته ارائه میدهد)، مقداری محلول هادی الکتریکی جهت بستن مدار الکتریکی و یک تجهیز سنجش خاص برای نمایش و اندازه گیری میزان pH میباشد.
سنسور pH در نوک خود دارای غشاء نازکی از شیشه حساس به هیدروژن میباشد که در انتهای داخلی تیوپ شیشهای قرار گرفته است. این تیوپ با الکترولیت بافر و سیم Ag/AgCl پر شده است. این بخش از الکترود را نیم سلول pH مینامند. سیستم مکمل قرار گرفته درون همین الکترود، ولتاژ ثابتی را تولید میکند و شامل سیم Ag/AgCl و محلول الکترولیت غنی شده با AgCl میشود. بر روی الکترود فیلتر کوچک نیز که اغلب از جنس سرامیک متخلخل است قرار گرفته است و تیوپ(نیم سلول مرجع) را به نمونه خارجی (نمونه تحت آزمایش) متصل مینماید.
واحد محاسباتی دستگاه های pH سنج، میزان pH را بر اساس اختلاف میزان ولتاژ اندازه گیری شده بین نیم سلول pH و نیم سلول مرجع بر حسب میلی ولت DC اندازه گیری می نماید، سپس مقدار اندازه گیری شده به وسیله واحد سنجش خوانده شده و به صورت mV یا pH بر روی نمایشگر به نمایش در خواهد آمد.
میزان mV اندازه گیری شده به وسیله الکترودpH از فرمول Nernst پیروی میکند:
در اینجا:
Eobs= پتانسیل الکتریکی مشاهده شده
Ec = پتانسیل الکتریکی نیم سلول مرجع
+AH = فعالیت یون هیدروژن
T = دما به درجه کلوین
n = ظرفیت یون اندازه گیری شده (۱)
F = ضریب ثابت فارادای (۹٫۶۴۸۵×۱۰۴)
R= ثابت گاز (۸٫۳۱۴۳۲) به کلوین
از این مبادله میتوان این طور استنباط کرد که اگر دما T تغییر کند، عبارت ln(10)RT / nF همان فاکتور شیب، نیز تغییر میکند. جدول زیر تغییر در فاکتور شیب را برای تغییرات دما نشان میدهد.
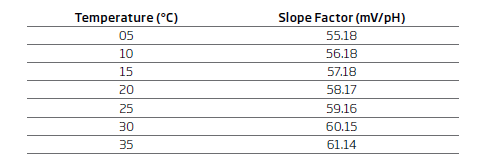
چطور دما روی pH محلول تاثیر میگذارد
pH یک محلول یا یک نمونه تابعی از دمای محلول است. اما چرا؟
علت را میتوان در تغییرات میزان تفکیک یونی و افزایش فعالیت یون های یک محلول با تغییرات دما جستجو کرد. به عنوان مثال:
در دمای اتاق pH آب تقریباً برابر ۷ میباشد و این یعنی حدود ۷-۱۰ مول از یون+ H در هر لیتر آب در دمای اتاق موجود است. اما با افزایش دما توانای آب برای یونیزه کردن سایر مولکول ها، اتم ها و یون ها، کریستال ها و … افزایش میابد لذا غلظت یون های هیدروژن و فعالیت آن ها افزایش میاید. نمونه بارز دیگر این مسئله بافرهای استاندارد pH هستند که مقادیر آن کاملاً مشخص است، روی بسته های بافر شما میتواند میزان تغییرات در میزان pH را با تغییرات دما مشاهده نمایید.
مثال دیگر تغییر pH با تغییر دما آب خالص است. در آب خالص با تغییر دما بین ۰ تا ۱۰۰ درجه سانتیگراد تغییرات pH را به مقدار تقریبی ۱٫۳pH مشاهده خواهیم نمود. این مثال نشان میدهد که حتی مایعهای خنثی هم میتوانند ضریب حرارتی بالایی داشته باشند.
تمام نمونهها دارای ضریب حرارتی متفاوتی هستند و تغییر در میزان pH به خاطر تغییر در ضریب دمای نمونه قابل جبران نیست. البته این مسئله یک استثنا دارد، از آنجایی که رفتار بافرها با تغییرات دما به خوبی ساخته شده هستند، در pH متر های هوشمند که دارای توانایی جبرانسازی اتومات هستند، مقدار تغییر pH به واسطه دما جبرانسازی میگردد.
عدد pH نوشته شده بر روی بافر ها در ۲۵درجه سانتیگراد در نظر گرفته شده است، لذا اگر در زمان کالیبراسیون تغییری در دما ایجاد شود، با سنجش دما میتوان مقدار واقعی pH را بدست آورد.
خواهشمند است با ثبت نظرات ارزشمند خود، ما را در بهتر نمودن فعالیت مجله اینترنتی مان یاری نمایید.
با تشکر از وقت شما
هانا-ایران|Hanna-Iran
نماینده انحصاری محصولات هانا در ایران
پایان قسمت اول
تهیه کننده: ح.رضاپور












